§ 31. Генетика и здоровье человека
Подробное решение параграф § 31 по биологии для учащихся 10 класса, авторов Сивоглазов В.И., Агафонова И.Б., Захарова Е.Т. Базовый уровень 2014
Вспомните!
Что такое мутагены?
Мутагены – это факторы среды, влияющие на организм и вызывающие мутации.
Какие наследственные заболевания вам известны?
Фенилкетонурия
Серповидноклеточная анемия
Гемофилия
Альбинизм
Дальтонизм
Синдром Дауна
Вопросы для повторения и задания
1. Как влияют соматические мутации на здоровье людей?
Мутации, которые возникают в соматических клетках тела, вызывают преждевременное старение, сокращают продолжительность жизни, а также, в зависимости от места возникновения, влияют на определённые жизненно важные функции организма. Соматические мутации представляют очень серьёзную угрозу здоровью населения, так как это первый шаг к образованию злокачественных опухолей. Подавляющее число всех случаев заболевания раком молочной железы — результат соматических мутаций. Под влиянием мутагенов количество изменений наследственного материала резко увеличивается. После аварии на Чернобыльской АЭС (1986 г.) в результате радиационного воздействия частота заболеваний раком щитовидной железы в Гомельской области возросла в 20 раз. Избыточное ультрафиолетовое излучение повышает риск возникновения рака кожи.
2. Каковы последствия возникновения генеративных мутаций?
Генеративные мутации, т. е. нарушения структуры ДНК в половых клетках, могут приводить к спонтанным абортам (выкидышам), мертворождению и к увеличению частоты наследственных заболеваний. Причём, если эти мутации не вызывают гибели организма и не ведут к серьёзным нарушениям репродуктивной функции, они будут передаваться из поколения в поколение, постепенно увеличивая частоту встречаемости в популяции.
3. Назовите известные вам наследственные заболевания человека. Каковы их причины?
Фенилкетонурия — рецессивное заболевание, которое возникает в результате мутации гена, расположенного в 12–й хромосоме, и приводит к накоплению в организме человека избытка аминокислоты — фенилаланина. При отсутствии строгой диеты, исключающей продукты, содержащие фенилаланин, у ребёнка может развиться умственная отсталость.
К рецессивным болезням относится альбинизм — врождённое отсутствие пигментации кожи, волос и радужки глаз.
Замена всего одного нуклеотида в молекуле ДНК, приводящая к изменению структуры молекулы гемоглобина, вызывает серповидноклеточную анемию. В крови таких больных обнаруживаются эритроциты серповидной формы, не способные нормально переносить кислород.
Если мутантный ген является доминантным и подавляет «нормальный» аллельный ген, то говорят об аутосомно-доминантном заболевании. Примером такой болезни является синдром Марфана.
Примером заболеваний, которые наследуются сцепленно с полом, может служить одна из форм гемофилии — нарушение свёртываемости крови.
Изменения числа хромосом, как правило, возникают в результате нерасхождения гомологичных хромосом в процессе образования половых клеток одного из родителей и вызывают серьёзные нарушения развития. Самой распространённой патологией такого рода является болезнь (синдром) Дауна.
Лишняя 13- я хромосома приводит к развитию синдрома Патау, который характеризуется столь тяжёлыми отклонениями в развитии, что 95% больных детей умирает в первый год жизни.
Дополнительная Х-хромосома у мужчин (ХХY) вызывает развитие синдрома Клайнфельтера, который выражается в бесплодии, женском типе скелета (широкий таз, узкие плечи), нарушении умственного развития.
Отсутствие одной Х-хромосомы у женщин (Х0) приводит к развитию синдрома Шерешевского—Тернера. Женщины, имеющие такой хромосомный набор, бесплодны, имеют широкую грудную клетку, короткую шею и рост в среднем не более 150 см. Интересно, что женщины с лишней Х-хромосомой (ХХХ) не имеют практически никаких физических отличий от здоровых женщин, однако у них чаще наблюдаются отклонения в поведении и трудности в обучении.
Самой известной хромосомной мутацией у человека является утрата фрагмента 5- й хромосомы, которая приводит к развитию синдрома «кошачьего крика». Признаком его служит необычный плач, напоминающий мяуканье кошки, что связано с нарушением строения гортани и голосовых связок. Кроме того, у таких детей наблюдается умственное и физическое недоразвитие.
4. Какова главная задача медико-генетического консультирования? Есть ли в вашем населённом пункте медико-генетическая консультация? Если нет, узнайте, где находится ближайшая подобная организация. Выясните, какие методы диагностики в ней применяются.
Да, есть. Значительно снизить вероятность возникновения наследственных заболеваний позволяет медико-генетическое консультирование. Главная задача такого консультирования заключается в прогнозировании появления детей с той или иной наследственной аномалией. Поводом для консультирования могут стать близкородственные браки, работа супругов на вредном предприятии или наличие родственников, имеющих наследственные заболевания. При наличии в семье наследственных заболеваний врач-консультант составляет подробную родословную, на основании которой часто можно определить тип наследования данного заболевания и рассчитать вероятность рождения больного ребёнка. Если в консультацию обращается супружеская пара, у которой уже родился ребёнок с наследственной патологией, работа начинается с постановки точного диагноза, после чего определяют величину риска рождения второго больного ребёнка. Современные методы позволяют исследовать генотипы родителей с целью обнаружения конкретной мутации.
5. Что относится к методам дородовой (пренатальной) диагностики?
Ультразвуковое обследование плода, взятие крови из пуповины и анализ околоплодной жидкости, в которой всегда есть клетки эмбриона и продукты его метаболизма, позволяют на ранних этапах беременности обнаружить наследственные заболевания. Если диагностируется болезнь, способы лечения которой на сегодняшний день не разработаны, родители могут принять решение о прерывании беременности. В настоящее время риск рождения детей с наследственными заболеваниями может быть значительно снижен с помощью генетического консультирования и пренатальной диагностики. Применение лекарственных препаратов, корректирующих нарушенную функцию, или соблюдение определённой диеты, как в случае фенилкетонурии, позволяют компенсировать проявление многих мутаций. Последние достижения генной терапии по введению в клетки больного нормальной копии повреждённого гена позволяют надеяться, что проблема лечения многих наследственных заболеваний в будущем будет решена.
Подумайте! Вспомните!
1. Как вы считаете, в чём заключается опасность близкородственных браков?
Зачастую особи являются гетерозиготами по многим признакам, тем самым признаки каких-либо заболеваний находящихся в рецессивном состоянии есть у родственников. При вступлении в брак таких людей, возникает вероятность то, что мутации из рецессивного состояния перейдет в доминантное гомозиготное состояние. При этом увеличивается риск наследственных заболеваний у потомков таких браков. Поэтому во многих странах такие браки запрещены.
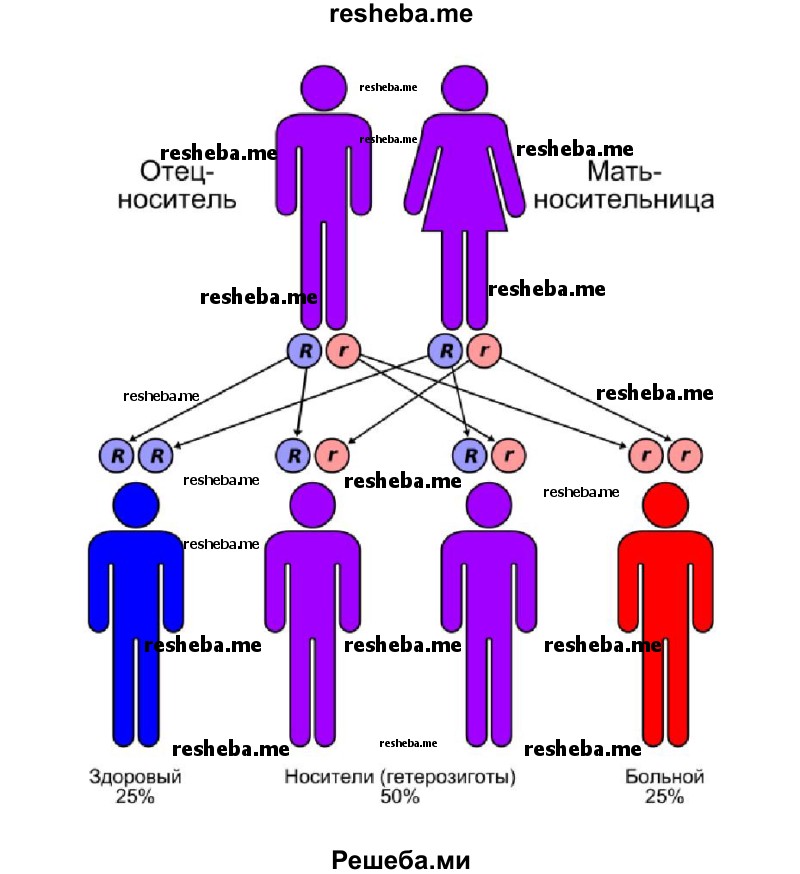
2. Подумайте, в чём особенность изучения наследования признаков у человека.
Человек является особенным объектом генетических исследований. К нему неприменим основной метод генетики — гибридологический. Малочисленное, а порой единичное потомство затрудняет применение статистических методов в пределах одной семьи. Большая продолжительность жизни, сопоставимая с жизнью самого исследователя, и поздние сроки наступления половой зрелости тоже являются ограничивающими факторами для использования классических генетических методов. В связи с этим в настоящее время для изучения генетических особенностей человека используют специальные методы. Существует четыре основных метода генетики человека: цитогенетический, близнецовый, генеалогический и популяционно- статистический. Наряду с ними используют и другие методы, основанные в первую очередь на современных достижениях биохимии и молекулярной биологии.
3. Почему хозяйственная деятельность человека увеличивает мутагенное влияние среды?
Так как человек активно использует гербициды, пестициды, генно-модифицированные организмы, так же электромагнитные, ренгеновские, гамма-лучи, элементарные частицы. Все это и другие факторы влияют на самого человека.
4. Используя дополнительную литературу и ресурсы Интернета, подготовьте сообщение или презентацию о современных достижениях в области диагностики и лечения наследственных заболеваний.
Наследственным заболеваниям свойственны различные клинические проявления, и их лечение во многом является симптоматическим. Отдельные нарушения метаболизма исправляют назначением специальных диет, направленных на уменьшение токсических веществ в организме, накопление которых обусловлено мутациями в определённых генах. Например, при фенилкетонурии назначают безаланиновую диету.
Для ослабления симптомов наследственных болезней, связанных с дефектом определённого белка, вводят внутривенно такую его функциональную форму, которая не вызывает иммунной реакции. Такая замещающая терапия применяется при лечении гемофилии, тяжёлого комбинированного иммунодефицита и др. Иногда для компенсации определённых утраченных функций проводят трансплантацию костного мозга и других органов. Существующая терапия в подавляющем большинстве случаев мало эффективна, а само лечение следует проводить многократно, несмотря на его высокую стоимость.
Принципиально новым методом, эффективным и направленным на уничтожение генетической причины наследственного заболевания, является генотерапия. Суть метода генотерапии – введение нормальных генов в дефектные соматические клетки. Концепция генной терапии заключатся в том, что наиболее радикальным способом борьбы с разного рода заболеваниями, вызываемыми изменениями генетического содержания клеток, должна быть обработка, направленная непосредственно на исправление или уничтожение самой генетической причины заболевания, а не её следствий. В связи с тем, что генная терапия представляет собой новое направление медицинской генетики, а болезни, которые пытаются лечить этим способом, очень разнообразны, создано множество оригинальных методических подходов к этой проблеме. В настоящее время исследования по генотерапии в основном направлены на коррекцию генетических дефектов соматических, а не половых клеток, что связано с чисто техническими проблемами, а также из соображений безопасности.
5. «Генная терапия — медицина будущего». Согласны ли вы с этим утверждением? Аргументируйте свою точку зрения. Примите участие в дискуссии на эту тему.
Лечение заболеваний с помощью генов получило название генотерапии. Сейчас в мире насчитывается порядка 400 проектов, посвященных лечению с помощью генотеропии. Разработке программы генной терапии предшествуют тщательный анализ тканеспецифической экспрессии соответствующего гена, идентификация первичного биохимического дефекта, исследование структуры, функции и внутриклеточного распределения его белкового продукта, а также биохимический анализ патологического процесса. Все эти данные учитываются при составлении соответствующего медицинского протокола.
Апробацию процедуры генокоррекции наследственного заболевания проводят на первичных культурах клеток больного, в которых в норме функционально активен данный ген. На этих клеточных моделях оценивают эффективность выбранной системы переноса экзогенной ДНК, определяют экспрессию вводимой генетической конструкции, анализируют ее взаимодействие с геномом клетки, отрабатывают способы коррекции на биохимическом уровне. Используя культуры клеток, можно разработать систему адресной доставки рекомбинантных ДНК, однако проверка надежности работы этой системы может быть осуществлена только на уровне целого организма. Поэтому такое внимание в программах по генной терапии уделяется экспериментам in vivo на естественных или искусственно полученных моделях соответствующих наследственных болезней у животных.
Успешная коррекция генетических дефектов у таких животных и отсутствие нежелательных побочных эффектов генной терапии являются важнейшей предпосылкой для разрешения клинических испытаний. Таким образом, стандартная схема генокоррекции наследственного дефекта включает серию последовательных этапов. Она начинается созданием полноценно работающей (экспрессирующейся) генетической конструкции, содержащей смысловую (кодирующую белок) и регуляторную части гена. На следующем этапе решается проблема вектора, обеспечивающего эффективную, а по возможности и адресную доставку гена в клетки-мишени. Затем проводится трансфекция (перенос полученной конструкции) в клетки-мишени, оценивается эффективность трансфекции, степень коррегируемости первичного биохимического дефекта в условиях клеточных культур (in vitro) и, что особенно важно, in vivo на животных - биологических моделях. Только после этого можно приступать к программе клинических испытаний.
Существует два типа генотерапии: заместительная и корректирующая.
Заместительная генотерапия заключается во вводе в клетку неповрежденного гена. Внесенная копия заменит по функциям сохранившийся в геноме больного дефектный ген. Все проводимые сегодня клинические испытания используют внесение в клетку дополнительных количеств ДНК.
При корректирующей терапии предполагается замена дефектного гена нормальным в результате рекомбинации. Пока этот метод на стадии лабораторных испытаний, так как эффективность его еще очень низка, но последние исследования показывают успехи в лечении некоторых заболеваний.
6. Подготовьте доклад (реферат или презентацию) на тему «Наследственные аномалии человека, обусловленные генными, хромосомными или геномными мутациями. Причины роста числа наследственных аномалий в человеческой популяции».
Появление наследственных болезней может быть связано с тремя причинами. Первый источник мутаций - нарушение хромосом (утеря одной из 46 хромосом или добавление лишней приводит к серьезным изменениям в развитии человека). Во-вторых, происходят изменения структуры хромосом в половых клетках родителей. И, наконец, генные мутации.
Из 23 пар хромосом одну пару представляют половые и 22 - аутосомные, которые различаются между собой по размеру и форме. Добавление одной из хромосом (трисомия) или ее отсутствие (моносомия) приводят к разнообразным конституционным изменениям. Анализ кариотипов, проведенный сразу же после того, как научились распознавать «в лицо» каждую хромосому человека, дал возможность выявить целый ряд наследственных болезней, связанных с изменением баланса определенной хромосомы.
В 1866 г. была обнаружена болезнь Дауна, характеризующаяся идиотизмом и целым комплексом аномалий. Она хорошо диагностируется с первых лет жизни. Скандинавские, североамериканские и японские цитогенетики впервые в 1959 г. установили, что болезнь связана с трисомией по очень маленькой 21-й хромосоме. Дети с синдромом Дауна рождаются с достаточно высокой частотой - один на 750 новорожденных. Они чаще встречаются у сравнительно пожилых матерей (со средним возрастом 35 лет). У больных маленькая головка, плоское лицо с выступающими скуловыми дугами, узкие глазные щели, маленький пуговчатый нос. Внешне они очень неуклюжи, умственная отсталость резко выражена, они, как правило, бесплодны.
Трисомия по другим хромосомам встречается гораздо реже. Во всех случаях наблюдается отклонение от нормы физических признаков и умственная депрессия. Выявлены новорожденные, у которых есть дополнительная 8-я хромосома (аномалии тела и низкий уровень интеллекта), 9-я (нарушение костей скелета и суставов, пороки сердца, аномалии почек и мочевыводящих путей), 13-я (синдром Патау, сопровождающийся нарушениями в строении головного мозга и лица), 18-я (синдром Эдвардса, характеризующийся недоразвитием костной системы и пороками сердца), 22-я хромосома (отставание в физическом и умственном развитии).
Выявлены также случаи частичной трисомии и моносомии. Все это больные, неполноценные люди с различными типами нарушения развития физических и психических признаков.
Присутствие второй Х-хромосомы определяет полноценное развитие яичников и половых органов по женскому типу. Образование первичных половых закладок в направлении мужского пола определяется наличием в хромосомном наборе Y-хромосомы. Нарушение баланса половых хромосом приводит к глубоким изменениям организмов. При наличии только одной половой хромосомы X происходит ненормальное развитие женского плода. Возникающую в результате нарушения хромосомного набора патологию впервые описал в 1925 г. русский врач Н. А. Шерешевский (синдром Шерешевского-Тернера). Он проявляется в малом росте, медленном половом развитии, бесплодии, наличии своеобразных кожных складок на шее.
У кариотипа с двумя Х- и одной Y-хромосомой развивается плод мужского пола с рядом недостатков. Это нарушение баланса хромосом было установлено в 1942 г. и получило название синдрома Клейнфельтера. Он выражается в сильном ослаблении сперматогенеза, почти полном бесплодии, инертности и умственной отсталости. При высоком росте больные имеют женский тип строения скелета и тела, у них недоразвиты вторичные половые признаки.
Иная клинико-генетическая структура у лиц с двумя Y- и одной Х-хромосомой. По обобщенным данным такие случаи встречаются с частотой один на тысячу новорожденных мальчиков. Внешне это мужчины с нормальным физическим и умственным развитием, обычно высокого роста. Людей с добавочной Y-хромосомой часто выявляли среди правонарушителей, что дало повод высказать предположение об определенных отклонениях у некоторых из них в социальном поведении.
При массовом обследовании новорожденных, детей школьного возраста и психически больных людей были выявлены лица женского пола с тремя Х-хромосомами. Они имеют нормальное физическое и умственное развитие, нормальную плодовитость и по внешним признакам их трудно выделить. У некоторых из таких женщин описаны изменения в половой системе. Аномалии развития встречаются редко. Но они чаще, чем обычные люди, страдают шизофренией.
Увеличение числа дополнительных Х-хромосом приводит к нарастанию отклонений от нормы. Но даже женщины с двумя лишними хромосомами могут дать нормальное потомство. В большинстве же случаев при двух и трех дополнительных Х-хромосомах женщины умственно неполноценны, у них наблюдаются отклонение в системе половых органов, изменение скелета, аномалии зубов и черепно-лицевая дисморфия.
В большом количестве случаев наблюдалось изменение размеров различных хромосом за счет дупликации отдельных участков или их утери. Такие отклонения часто приводят к наследственной патологии. Установлены аномалии скелета, деформации мозговой и лицевой частей черепа, пороки сердца. Частичная дупликация 13-й хромосомы вызывает синдром «кошачий глаз», сочетание двух врожденных пороков развития - дефекта радужной оболочки глаза и атразии анального отверстия.
Другой сходный по названию синдром «кошачий крик» обусловлен потерей участка 5-й хромосомы. У детей с этим синдромом поражена нервная система, нарушено строение гортани, что создает специфический для болезни плач. Утеря участка 11-й хромосомы приводит к проявлению синдрома отсутствия радужной оболочки глаза и другим глазным аномалиям (глаукома, катаракта, помутнение роговицы). Частичная потеря 18-й хромосомы приводит к умственной отсталости, задержке физического развития, лицевым дисморфиям.
Основная часть наследственных болезней человека связана с генными мутациями, при которых одно азотистое основание заменено другим. Например, серповидноклеточная анемия вызвана изменением всего лишь одного азотистого основания среди 1500, входящих в состав гемоглобина. В результате из 300 аминокислот кодируемого белка включается одна иная аминокислота. Глобин теряет способность к транспорту кислорода, и дети при рождении погибают.
Выявление генных мутаций и исследование характера их наследования наиболее успешно осуществляется на основе анализа биохимического состава гена. О мутации гена судят косвенно, по его белковому продукту. Для структурных белков определяют количественное соотношение и типы полипептидных субъединиц, электрофоретическую подвижность. Примером установления первичного биохимического дефекта при наследственной патологии может быть группа болезней накопления гликозамипогликанов мукополи-сахаридозы. В 1952 г. были описаны два синдрома этих болезней - Гурлер и Хантера.
Оказалось, что основные клинические проявления синдромов связаны с накоплением в клетках и основном межклеточном веществе многих органов, костной и мягкой соединительной ткани мукополисахаридов. Избыточное содержание этих полимеров происходило из-за отсутствия их расщепления в специальных органеллах клетки - лизосомах. Исследования биохимических характеристик гликозамипогликанов позволили идентифицировать в тканях человека девять типов мукополи-сахаридозов при разных формах болезней.
Диагностика генных мутаций у человека связана с изучением конкретного клинического и биохимического врожденного дефекта. Измеряется активность того или иного фермента. При массовых обследованиях, в частности среди новорожденных, используют скрининг-программы (диагностика наследственных заболеваний). В крови или моче выявляют вещества, которые в норме не встречаются в больших количествах. Может возникнуть также дефицит продукта определенной реакции. Например, у лиц с наследственной болезнью Мак-Ардля наблюдается дефект фермента фосфорилазы, расщепляющего гликоген. В связи с этим при мышечной нагрузке концентрация молочной кислоты - конечного продукта распада глюкозы - в отличие от нормы не увеличивается.
Теоретически возможна мутация по любому структурному или регуляторному участку гена каждого фермента. Уже известно более 100 генных мутаций по определенным ферментным генам. Кроме того, предполагают, что некоторые из ферментных дефектов ведут к гибели особи на ранней стадии развития.
Врожденным дефектом цистатионинсинтетазы - фермента, участвующего в образовании цистатиона, вызывается гомоцистинурия. Этот фермент выполняет важную функцию в нервной системе. У людей с гомоцистинурией длинные конечности, костлявая фигура. У них ослаблены соединительнотканные связки скелета, разболтаны суставы, наблюдаются вывихи хрусталика глаза, приводящие к плохому зрению, встречается умственная отсталость.
Обнаружены также мутации генов ферментов углеводного обмена. Известны гликогенозные заболевания, вызванные дефектом различных ферментов, участвующих в распаде гликогена, образовании и переработке глюкозы. Происходит избыточное отложение гликогена в скелетной мускулатуре, сердечной мышце и печени. Гликогенозы могут приводить к умственной отсталости, печеночной недостаточности и мышечной слабости. Другой пример нарушения углеводного обмена - галактозимия. Она связана с недостаточной активностью галактозо-1-фосфотуридилтрапсферазы. Этот фермент переводит в кишечнике молочный сахар (галактозу) в глюкозу и в таком виде утилизируется организмом. Если этот путь метаболизма галактозы, которая входит в состав материнского молока, нарушен, в организме ребенка накапливается галактоза и ее фосфат. В результате происходит расстройство нервной системы ребенка, с самого рождения наблюдаются сильная желтуха, поражение печени и селезенки, умственная отсталость, возможна даже смерть.
Наследственные болезни липидозы характеризуются нарушением обмена жиров и жироподобных веществ (липидов). Они сопровождаются тяжелыми нарушениями умственных способностей, расстройством жизненно важных функций нервной системы.
Наряду с болезнями, вызванными мутациями отдельных генов, есть заболевания, связанные с нарушением комплекса генов. В этих случаях степень проявления болезни определяется различной комбинацией генов. Такие болезни широко распространены, их относят к наследственно предрасположенным. Наибольшее значение среди них имеют атеросклероз, гипертоническая болезнь, сахарный диабет, некоторые психические болезни. Их проявление в большой мере зависит от влияния внешней среды. Избыточное питание, длительное перенапряжение нервной системы, психические травмы способствуют развитию атеросклероза. Сахарный диабет связан с недостатком инсулина. Генотерапия основана на ежедневном введении в организм человека дефицитного гормона.
7. Оцените уровень информированности населения вашего района о роли медико-генетического консультирования в формировании будущего здоровья нации. Обсудите результаты с одноклассниками, сделайте выводы и представьте их для ознакомления общественности.
Медико-генетическое консультирование - специализированный вид медицинской помощи - является наиболее распространенным видом профилактики наследственных болезней. Суть его заключается в определении прогноза рождения ребенка с наследственной патологией, объяснении вероятности этого события консультирующимся и помощи семье в принятии решения о дальнейшем деторождении.
Еще в конце 20-х годов С.Н.Давиденков в России, впервые в мире организовал медико-генетическую консультацию при Институте нервно-психиатрической профилактики. Он четко сформулировал задачи и методы медико-генетического консультирования. Однако развитие данной области профилактики и генетики человека в целом затормозилось в 30-х годах практически во всех развитых странах. Это было связано с тем, что в нацистской Германии для обоснования геноцида использовали генетические концепции и ввели насильственную стерилизацию как метод "оздоровления расы". В Москве был закрыт Медико-генетический институт. В США медико-генетические консультации (кабинеты) начали организовываться в 40-х годах, но действительно интенсивное развитие такой помощи в разных странах (в том числе в России и Германии) началось в 60-70-х годах. К этому времени уже отмечался большой прогресс в изучении хромосомной патологии и наследственных болезней обмена веществ. Термин "медико-генетическая консулътация" определяет два понятия:
1) консультация врача-генетика как врачебное заключение;
2) структурное подразделение в каком-либо звене здравоохранения (при больнице, при объединении, поликлинике и др.).
Показаниями для медико-генетического консультирования являются:
1) рождение ребенка с врожденным пороком развития;
2) установленная или подозреваемая наследственная болезнь в семье в широком смысле слова;
3) задержка физического развития или умственная отсталость у ребенка;
4) повторные спонтанные аборты, выкидыши, мертворождения;
5) близкородственные браки;
6) воздействие подозреваемых на тератогенность или известных тератогенов в первые 3 мес. беременности;
7) неблагополучное протекание беременности. В принципе каждая супружеская пара должна пройти медико- генетическое консультирование до планирования деторождения (проспективно) и безусловно после рождения больного ребенка (ретроспективно).
В настоящее время такой тип консультирования набирает обороты, так как мутагенных факторов, вызывающих различные заболевания становится все больше.